Jaki jest wpływ pH na organiczne reakcje pośrednie?
Zostaw wiadomość
Hej tam! Jako dostawca organicznych półproduktów widziałem na własne oczy, jak istotna jest koncepcja pH w świecie organicznych reakcji pośrednich. Na tym blogu omówię wpływ pH na te reakcje i wyjaśnię, dlaczego jest to dla Ciebie ważne, niezależnie od tego, czy zajmujesz się badaniami, czy produkcją.
Zrozumienie podstaw pH
Zanim zagłębimy się w wpływ na organiczne reakcje pośrednie, przyjrzyjmy się szybko, czym jest pH. pH jest miarą tego, jak kwasowy lub zasadowy jest roztwór. Mierzy się go w skali od 0 do 14, gdzie 0 oznacza bardzo kwaśny, 7 oznacza obojętny (jak czysta woda), a 14 oznacza wysoce zasadowy.
pH roztworu może mieć ogromny wpływ na zachowanie cząsteczek. W chemii organicznej wiele reakcji obejmuje naładowane cząsteczki lub cząsteczki, które w zależności od pH mogą zostać protonowane (uzyskać jon wodorowy) lub deprotonowane (utracić jon wodorowy).
Wpływ na szybkość reakcji
Jednym z najbardziej znaczących wpływów pH na organiczne reakcje pośrednie jest szybkość reakcji. Przebieg wielu reakcji organicznych zależy od obecności określonych naładowanych substancji. Na przykład w reakcji katalizowanej kwasem proton (H⁺) często bierze udział w etapie określającym szybkość.
Załóżmy, że mamy reakcję hydrolizy estrów. W warunkach kwaśnych (niskie pH) tlen karbonylowy estru może ulegać protonowaniu. To protonowanie sprawia, że węgiel karbonylowy jest bardziej elektrofilowy, co oznacza, że jest bardziej prawdopodobne, że zareaguje z nukleofilem (w tym przypadku z wodą). Szybkość reakcji wzrasta, ponieważ etap protonowania aktywuje ester w kierunku ataku nukleofilowego.
Natomiast w warunkach zasadowych (wysokie pH) reakcja przebiega według innego mechanizmu. Jony wodorotlenkowe (OH⁻) działają jak nukleofil i bezpośrednio atakują węgiel karbonylowy. Szybkość tej reakcji zależy także od stężenia jonów OH⁻, które jest powiązane z pH roztworu.
Wpływ na mechanizmy reakcji
pH może również zmienić sam mechanizm reakcji. Weźmy reakcję aldehydu z aminą pierwszorzędową. W warunkach kwaśnych reakcja przebiega poprzez utworzenie iminy. Aldehyd jest najpierw protonowany, co czyni go bardziej elektrofilowym. Następnie amina atakuje protonowany aldehyd i po serii etapów tworzy się imina.
Natomiast w warunkach zasadowych reakcja może przebiegać inną drogą. Amina może działać jako zasada i deprotonować sąsiednią cząsteczkę, prowadząc do innego zestawu związków pośrednich i innego produktu końcowego.
Wpływ na stabilność półproduktów
Stabilność organicznych półproduktów zależy w dużym stopniu od pH. Niektóre półprodukty są stabilne w warunkach kwaśnych, ale szybko rozkładają się w warunkach zasadowych i odwrotnie.
Na przykład karbokationy to dodatnio naładowane półprodukty, które często powstają w reakcjach organicznych. Są na ogół bardziej stabilne w roztworach kwaśnych, ponieważ wysokie stężenie protonów może pomóc ustabilizować ładunek dodatni. W roztworach zasadowych karbokationy mogą reagować z jonami wodorotlenkowymi lub innymi nukleofilami, powodując ich szybki rozkład.
Selektywność w reakcjach
pH może również odgrywać kluczową rolę w selektywności reakcji. W reakcji, w której możliwych jest wiele produktów, dostosowanie pH może sprzyjać tworzeniu się jednego produktu w stosunku do innych.
Rozważmy reakcję, w której alkohol może ulec odwodnieniu (tworząc alken) lub utlenieniu (tworząc aldehyd lub keton). Na wybór pomiędzy tymi dwiema drogami może wpływać pH. W warunkach kwaśnych często preferowane jest odwodnienie, ponieważ protonowanie grupy hydroksylowej sprawia, że jest ona lepszą grupą opuszczającą. W warunkach zasadowych utlenianie może być bardziej prawdopodobne, jeśli obecny jest odpowiedni środek utleniający.
Prawdziwy - Światowy przykład: Pro - ksylan
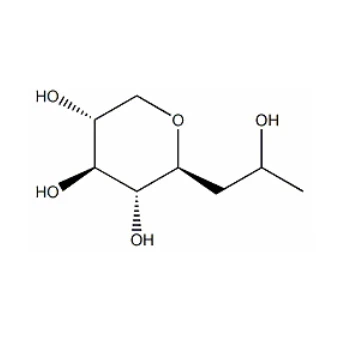
Porozmawiajmy teraz o przykładzie ze świata rzeczywistego.Pro - ksylanjest ważnym organicznym półproduktem stosowanym w przemyśle kosmetycznym. Synteza Pro-ksylanu składa się z kilku etapów, a kontrola pH ma kluczowe znaczenie na każdym etapie.
Na początkowych etapach syntezy wymagany jest określony zakres pH, aby zapewnić prawidłowe tworzenie kluczowych półproduktów. Te półprodukty są wrażliwe na zmiany pH. Jeśli pH jest zbyt wysokie lub zbyt niskie, reakcja może nie przebiegać zgodnie z oczekiwaniami, co prowadzi do niższych wydajności lub tworzenia się niepożądanych produktów ubocznych.
Dlaczego jest to ważne dla Ciebie jako kupującego
Jeśli działasz na rynku organicznych półproduktów, takich jak Pro-ksylan, zrozumienie roli pH w ich syntezie jest niezbędne. Pomoże Ci to ocenić jakość kupowanych produktów. Dostawca, który dobrze radzi sobie z kontrolą pH, ma większe szanse na wytworzenie wysokiej jakości półproduktów o stałych właściwościach.
Jeśli szukasz dostawcy półproduktów organicznych, potrzebujesz kogoś, kto może dostarczyć szczegółowych informacji na temat procesu produkcyjnego, w tym sposobu monitorowania i kontroli pH. Dzięki temu otrzymujesz najlepszy możliwy produkt do swojego zastosowania, niezależnie od tego, czy dotyczy to branży farmaceutycznej, kosmetycznej czy innej.
Kontakt w sprawie zakupów
Jeśli chcesz dowiedzieć się więcej na temat naszych półproduktów organicznych lub masz szczególne wymagania dotyczące swoich projektów, chętnie się z Tobą skontaktuję. Zależy nam na dostarczaniu produktów wysokiej jakości i doskonałej obsłudze klienta. Niezależnie od tego, czy potrzebujesz małej próbki do badań, czy dostawy na dużą skalę do produkcji, mamy wszystko, czego potrzebujesz. Skontaktuj się z nami i rozpocznijmy rozmowę o tym, jak możemy zaspokoić Twoje organiczne potrzeby pośrednie.
Referencje
- Smith, J. Chemia organiczna: nowoczesne podejście. Wydanie 3, Wydawnictwo, 2018.
- Jones, A. i in. „Rola pH w syntezie organicznej”. Journal of Organic Reactions, tom. 25, nie. 3.2020, s. 123 - 135.
- Podręcznik chemii kosmetycznej . Pod redakcją Browna, C., Wydawca, 2019.





